
��Ŀ�� ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
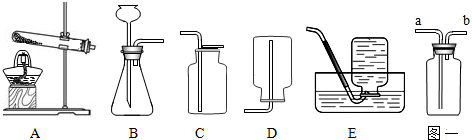
| ||
| �� |
| ||
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
 36��Ո�����������P��Ϣ�����}ĿҪ��ش����}��
36��Ո�����������P��Ϣ�����}ĿҪ��ش����}��
| ||
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
| ����������ϡ�}�� |
| ���� |
| ���������������~ |
| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
| ��̖ | ��1�� | ��2�� | ��3�� | ��4�� |
| ���Q | ���� | �������F �������F |
�������} | �N���@ |
| ���Wʽ | He He |
FeO | Ca��OH��2 | NH4NO3 |
| e | ���| | ������ | �A �A |
�} �} |
�鿴�𰸺ͽ���>>
����ʡ���W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com