
��Ŀ�� ��Դ�� �}�ͣ����x�}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
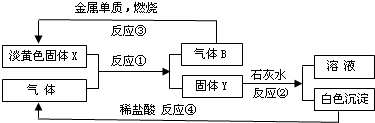
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
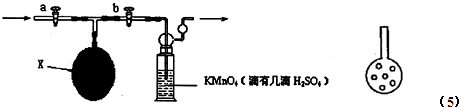
| �ζ� �Δ� | ��ȡKMnO4��Һ���w�e��mL�� | �˜ʲ�����Һ���w�e | ƽ��ֵ ��mL�� | ||
| �ζ�ǰ�̶� | �ζ���̶� | ���H�w�e��mL�� | |||
| ��һ�� | 5.00 | 0.00 | 19.60 | ||
| �ڶ��� | 5.00 | 0.20 | 19.60 | ||
| ������ | 5.00 | 0.06 | 18.06 | ||
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ����x�}
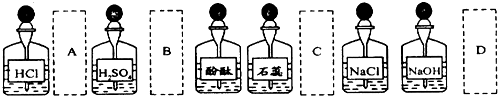
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ����x�}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
 2SO3��g����H=-98.3kJ?mol-1
2SO3��g����H=-98.3kJ?mol-1�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ����x�}
�鿴�𰸺ͽ���>>
����ʡ���W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com