
Ó}ńŅŃ–ĪŪ(įŁņ®īūįłļÕĹ‚őŲ)
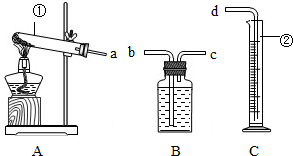

| ||
| ||
| ||
| ||
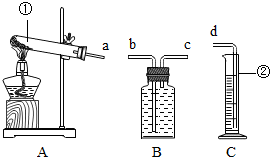
| ľ”üŠ |
| ľ”üŠ |
| Łc(di®£n)»ľ |
| Łc(di®£n)»ľ |
| ||
| °ų |
| ||
| °ų |
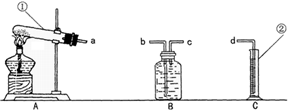
| ||
| ||
| ||
| ||
įŔ∂»÷¬–Ň - ĺöŃē(x®™)É‘(c®®)Ń–ĪŪ - ‘áÓ}Ń–ĪŪ
ļĢĪĪ °Ľ•¬ď(li®Ęn)ĺW(w®£ng)Ŗ`∑®ļÕ≤ĽŃľ–ŇŌĘŇeąů(b®§o)∆ĹŇ_(t®Ęi) | ĺW(w®£ng)…Ō”–ļ¶–ŇŌĘŇeąů(b®§o)Ć£Ö^(q®Ī) | Žä–Ň‘pÚ_Ňeąů(b®§o)Ć£Ö^(q®Ī) | …śöv ∑Őďüo(w®≤)÷ųŃx”–ļ¶–ŇŌĘŇeąů(b®§o)Ć£Ö^(q®Ī) | …ś∆ů«÷ôŗ(qu®Ęn)Ňeąů(b®§o)Ć£Ö^(q®Ī)
Ŗ`∑®ļÕ≤ĽŃľ–ŇŌĘŇeąů(b®§o)Žä‘í£ļ027-86699610 Ňeąů(b®§o)ŗ]Ōš£ļ58377363@163.com