
題目列表(包括答案和解析)
| 實驗次數 | 1 | 2 | 3 | 4 | 5 |
| 稀鹽酸的累計加入量 | 5.0g | 10.0g | 15.0g | 20.0g | 25.0g |
| 剩余固體的質量 | 2.0g | 1.5g | 1.0g | 0.5g | 0.5g |
| 實驗操作 | 預期現象與結論 |
| |
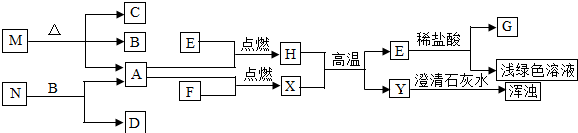
| B |
| 高溫 |
| ||
| ||
| ||
| ||
| ||
| ||
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com