
�}Ŀ�б�(�����𰸺ͽ���)
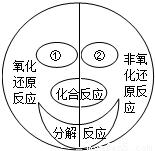 �ڷ���ǰ����Ԫ�ػ��σr�l(f��)��׃���Ļ��W��������������-߀ԭ��������D�ǻ��W�dȤС�Mͨ�^�����W���������ķN������������c����-߀ԭ�������Pϵ�D������(j��)�ˈDՈ�ش����І��}��
�ڷ���ǰ����Ԫ�ػ��σr�l(f��)��׃���Ļ��W��������������-߀ԭ��������D�ǻ��W�dȤС�Mͨ�^�����W���������ķN������������c����-߀ԭ�������Pϵ�D������(j��)�ˈDՈ�ش����І��}��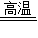 K2MnO4+MnO2+O2��
K2MnO4+MnO2+O2��  CO2+2H2O
CO2+2H2O 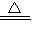 K2MnO4+MnO2+O2��
K2MnO4+MnO2+O2��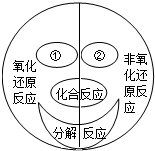 ��2013?�Җ|�hһģ���ڷ���ǰ����Ԫ�ػ��σr�l(f��)��׃���Ļ��W��������������-߀ԭ��������D�ǻ��W�dȤС�Mͨ�^�����W���������ķN������������c����-߀ԭ�������Pϵ�D������(j��)�ˈDՈ�ش����І��}��
��2013?�Җ|�hһģ���ڷ���ǰ����Ԫ�ػ��σr�l(f��)��׃���Ļ��W��������������-߀ԭ��������D�ǻ��W�dȤС�Mͨ�^�����W���������ķN������������c����-߀ԭ�������Pϵ�D������(j��)�ˈDՈ�ش����І��}��
| ||
| ||
| ||
| ||
| ||
 ij�о��ԌW��С�M�OӋ���M��������
ij�о��ԌW��С�M�OӋ���M��������
| ||
| ||
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com