
��Ŀ�� ��Դ�� �}�ͣ�����}
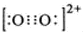 ��1mol O22+�к��еĦ��I��(sh��)Ŀ��2NA��
��1mol O22+�к��еĦ��I��(sh��)Ŀ��2NA���鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
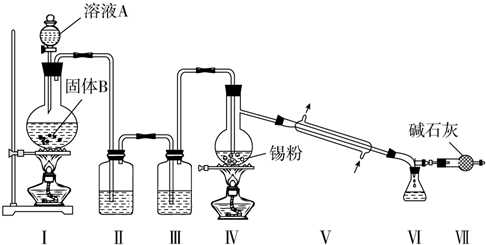
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | �٢� | B�� | �ޢ� | C�� | �ڢ� | D�� | �ۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | ߀ԭ�ԣ�F-��Cl-��Br-��I- | |
| B�� | ���ԣ�̼�ʯ̼�̼����c���������X | |
| C�� | �����ԣ�Na��S��F2��O2 | |
| D�� | NaHCO3��Һ��c��HCO3-����c��CO32-����c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | �״� | B�� | ���� | C�� | ��ȩ | D�� | ������� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}

�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | ��ϩ�c�Ț�ӳɣ�1��2-�������飩 | |
| B�� | ��ϩ�cˮ�ӳɣ��Ҵ��� | |
| C�� | �����|(zh��)�������Ț��c�����ڹ��l���·�����һ�����飩 | |
| D�� | Һ���c�����廯�F�������������屽�� |
�鿴�𰸺ͽ���>>
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com